LCĐT - Cục Quản lý Dược, Bộ Y tế vừa có văn bản thu hồi đối với lô thuốc dung dịch uống Batiwell trị nhiễm khuẩn đường hô hấp, làm loãng đờm do thuốc này vi phạm mức độ 2.
Cụ thể, thuốc dung dịch uống Batiwell (Bromhexin hydroclorid 0,8mg/ml), số GĐKLH: VD-31011-18, số kiểm soát: 00121, NSX: 08/03/2021, HD: 08/03/2024 do Công ty Cổ phần 23 tháng 9 sản xuất; mẫu thuốc do Trung tâm kiểm nghiệm thuốc - mỹ phẩm - thực phẩm thành phố Hà Nội lấy tại Công ty Cổ phần Dược phẩm Việt Nga (6A ngách 374 đường Âu Cơ, phường Nhật Tân, Tây Hồ, Hà Nội) không đạt tiêu chuẩn chất lượng về chỉ tiêu độ đồng đều thể tích và độ đồng đều hàm lượng (vi phạm mức độ 2).
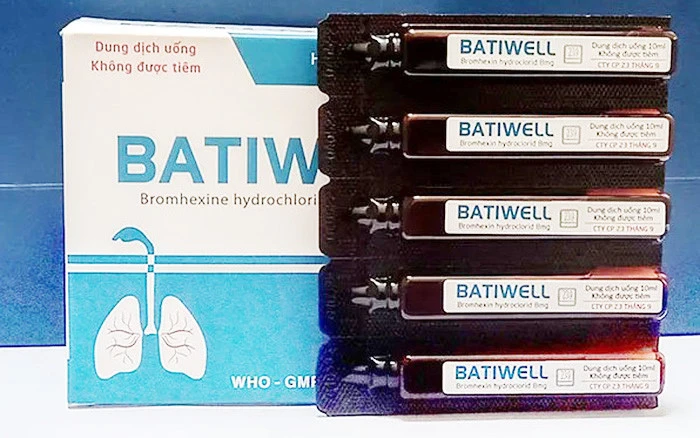 |
| Thuốc Batiwell trị nhiễm khuẩn đường hô hấp. |
Cục Quản lý Dược đã ra thông báo thu hồi toàn quốc lô thuốc dung dịch uống Batiwell, đồng thời yêu cầu Công ty Cổ phần 23 tháng 9 phối hợp với nhà phân phối, trong thời hạn 2 ngày kể từ ngày ký công văn gửi thông báo tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc về việc thu hồi lô thuốc dung dịch uống Batiwell; đồng thời tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng nêu trên; gửi báo cáo thu hồi về Cục Quản lý Dược.
Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, y tế các ngành cũng có trách nhiệm thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng này. Sở Y tế Hà Nội, Sở Y tế Thành phố Hồ Chí Minh kiểm tra và giám sát Công ty Cổ phần 23 tháng 9 thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.